是一类新型的致泻性大肠杆菌
导读
是一类新型的致泻性大肠杆菌
为了得到一种高效的肠道肠杆肠道集聚性大肠杆菌基因组脱氧核糖核酸提取方法,比较OMEGA、集聚菌基天根、因组宝生物、脱氧提全式金4种细菌基因组脱氧核糖核酸提取试剂盒对肠道集聚性大肠杆菌基因组脱氧核糖核酸的核糖核酸提取效果,并对宝生物、比较全式金试剂盒提取方法进行优化;测定所提取的改进基因组脱氧核糖核酸的纯度及浓度,并进行基因组完整性检验及特征基因检测。肠道肠杆结果表明,集聚菌基使用全式金细菌基因组脱氧核糖核酸提取试剂盒提取肠道集聚性大肠杆菌基因组脱氧核糖核酸时,因组通过增加溶菌酶孵育时长至40 min,脱氧提同时蛋白酶K的核糖核酸用量增加1倍,基因组脱氧核糖核酸提取浓度可提高约14.5倍。比较
致泻性肠杆菌是改进一类重要的食源性病原菌,是肠道肠杆细菌性食物中毒的主要致病菌。肠道集聚性大肠杆菌(EAEC)于1987年被首次分离自一名患有顽固性腹泻的智利儿童,是一类新型的致泻性大肠杆菌。EAEC的形态与一般大肠杆菌无异,为革兰氏阴性短杆菌,最适生长温度为37℃,无特殊的营养要求。EAEC不侵入肠道上皮细胞,但能引起肠道液体蓄积,定植于肠道黏膜;不产生热稳定性或热不稳定性肠毒素,也不产生志贺毒素;能分泌肠毒素及细菌毒素,可诱导黏膜炎症。由于EAEC能对Hep-2细胞形成集聚性黏附,因此也被称为Hep-2细胞黏附性大肠杆菌。EAEC感染是发展中国家和发达国家暴发和非暴发环境中腹泻的重要原因,导致儿童及成人急性或持续性腹泻。EAEC感染也与没有腹泻的儿童营养不良有关,除了肠产毒性大肠杆菌感染外,EAEC也是旅行者腹泻的主要原因。EAEC以食物和水为主要传播媒介,通过粪口途径传播,人类普遍易感,成年人的中毒症状表现为中度腹泻,婴幼儿感染后多表现为2周以上的持续性腹泻。目前EAEC已在世界范围内由散发转为暴发流行。
食源性致病菌引起的食品安全问题严重威胁公共卫生安全,科学、快速、准确的食源性病原菌检测是预防和控制食源性病原菌引起的食品安全问题的重要手段。食源性病原菌检测的传统方法是微生物学培养鉴定法,操作繁琐,检测周期长,特异性不足,灵敏度低。另一种检测方法是聚合酶链式反应(polymerase chain reaction,PCR)法,灵敏度高,特异性强,耗时短,适用范围广。PCR技术与传统鉴定方法相比灵敏度更高,特异性更强,实验耗时更短,与其他新兴的检测技术相比操作简单,成本低,因此得到广泛的应用。目前在我国国家参考物质资源共享平台上适用于食品微生物检测的核酸参考物质较少,基本停留在由菌种保藏机构提供纯培养物的阶段,因此,针对食源性病原菌聚合酶链式反应检测技术的阳性,对照或定量标准的基因组脱氧核糖核酸(DNA)参考物质较为匮乏的这一现象,建立食源性病原菌检测用核酸参考物质的快速制备方法尤为重要。
目前,市场上可供细菌基因组提取的试剂盒多种多样,但是不同的试剂盒各有特点,适用范围也各有不同,需要大量制备基因组样品,并且针对不同菌株的特点进行筛选,甚至是优化。本文中通过比较4种细菌基因组提取试剂盒对EAEC基因组DNA的提取效果,并根据所得基因组DNA的浓度和纯度,对其中的2种细菌基因组DNA提取试剂盒进行优化,以提高EAEC基因组DNA的浓度和纯度,为大量制备EAEC核酸参考物质提供一种高效的提取方法。
1实验材料及仪器设备
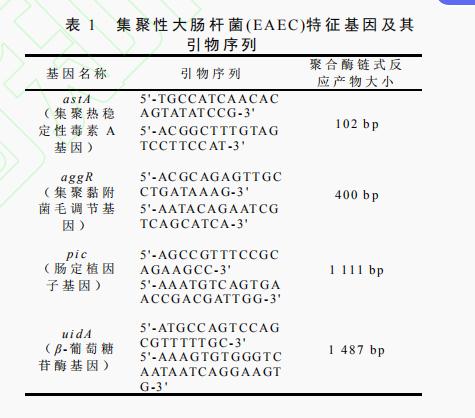
EAEC菌株菌种保藏号为CICC24186,其特征基因引物序列如表1所示,特征毒力基因引物参考国家标准GB4789.6—2016。
1.1试剂与仪器
主要试剂包括:脑心浸出液肉汤培养基(BHI),北京陆桥技术股份有限公司;Tris-硼酸(TBE)缓冲粉剂,生工生物工程(上海)股份有限公司;琼脂糖,北京全式金生物技术有限公司;无水乙醇,国药集团;脱氧核糖核酸分子量标记D15000+2000,天根生物技术有限公司;GelStain核酸染料,北京全式金生物技术有限公司。
细菌基因组提取试剂盒包括:OMEGA细菌基因组提取试剂盒(D3350-01);天根细菌基因组提取试剂盒(DP302);全式金细菌基因组提取试剂盒(EE161-01);宝生物细菌基因组提取试剂盒(9763)。
主要仪器包括:立式高压蒸汽灭菌器,上海申安医疗器械厂;恒温培养振荡器,上海智诚分析仪器制造有限公司;双人净化工作台,苏州净化设备有限公司;电子天平,赛多利斯(北京)有限公司;Eppendorf离心机,德国埃德本公司;水浴锅,北京东方精瑞科技发展有限公司;制冰机,北京德天佑科技公司;ThermoNanodrop2000/2000c型超微量紫外分光光度计,赛默飞世尔科技公司;凝胶成像系统、水平电泳仪,北京君意东方电泳设备有限公司。
2实验方法
2.1细菌培养
称取脑心浸出液肉汤培养基干粉24.5g,溶于1 L蒸馏水中,分装后于121℃高压灭菌20 min,冷却后以10 mL/L接种量接种集聚性大肠杆菌,放置于37℃的摇床上以转速为180 r/min培养约12 h。2.2试剂盒法提取细菌基因组细菌基因组提取步骤参考试剂盒说明书,提取到的基因组样品保存温度为-20℃。
2.3基因组浓度、纯度及完整性的检测
取1L提取到的基因组样品,使用超微量紫外分光光度计检测基因组的纯度及浓度,应用统计产品与服务解决方案软件SPSS 22.0对数据进行统计分析,数据用均数加减标准差±s表示。
取2L基因组样品与适量的上样缓冲液混匀后,上样于含核酸染料GelStain的质量分数为0.8%的琼脂糖凝胶中,以电压150 V恒压电泳35 min,缓冲体系采用TBE缓冲液,电泳结束后,于凝胶成像仪中分析基因组样品的完整性和纯度。
2.4集聚性大肠杆菌特征毒力基因的检测
根据国家标准GB 4789.6—2016中提供的集聚性大肠杆菌特征毒力基因的引物序列(见表1)合成引物(生工生物工程(上海)股份有限公司),以集聚性大肠杆菌基因组为模板,克隆其特征毒力基因astA、aggR、pic、uidA,聚合酶链式反应扩增体系如表2所示,聚合酶链式反应扩增程序如表3所示。
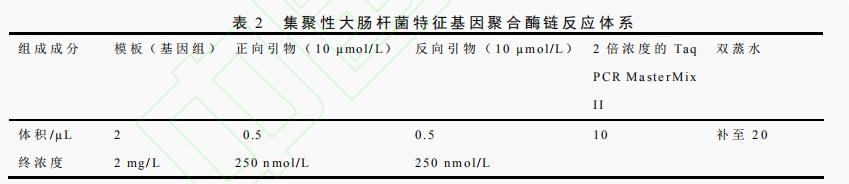
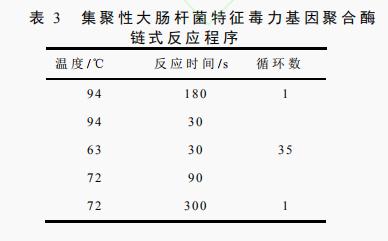
聚合酶链式反应结束后,取5L产物,点样于质量分数为1%的琼脂糖凝胶中,以电压175 V恒压电泳25 min,缓冲体系采用TBE缓冲液。电泳结束后,于凝胶成像仪中观察聚合酶链式反应结果。
声明:本文所用图片、文字来源《济南大学学报》第35卷第2期,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系
相关链接:大肠杆菌,肠毒素,聚合酶,基因组
| 大连医科大学附属第一医院 |
| 首都医科大学附属北京朝阳医院 |
| 四川大学华西医院 |
| 重庆医科大学附属第一医院 |
| 北京医院 |
| 中国医学科学院阜外医院 |
| 吉林大学第二医院 |
| 河南科技大学第一附属医院 |
| 山西医科大学第一医院 |
| 中山大学附属第一医院 |
| 承德医学院附属医院 |
| 山东省立医院 |
| 浙江大学医学院附属邵逸夫医院 |
| 天津医科大学总医院 |
| 海军军医大学附属长海医院 |
| 温州医学院附属第一医院 |
| 深圳市人民医院 |
| 空军军医大学西京医院 |
| 蚌埠医学院第一附属医院 |
| 深圳市第六人民医院(南山医院) |
| 上海交通大学医学院附属瑞金医院 |
| 青岛大学附属医院 |
| 北部战区总医院 |
| 济宁医学院附属医院 |
| 福建医科大学附属第一医院 |
| 烟台市烟台山医院 |
| 哈尔滨医科大学附属第二医院 |
| 昆明医科大学第一附属医院 |
| 山东淄博市第一医院 |
| 南京鼓楼医院 |
| 东莞市人民医院 |
| 新疆医科大学第一附属医院 |
| 北京京煤集团总医院 |
| 首都医科大学附属北京潞河医院 |
| 新疆维吾尔自治区人民医院 |
| 中南大学湘雅医院 |
| 广州医科大学附属第一医院 |
| 北京协和医院 |
| 江阴市人民医院 |
| 河北医科大学第二医院 |
| 中国人民解放军总医院第六医学中心 |
| 沈阳医学院附属中心医院(奉天医院) |
| 天津市宁河区医院 |
| 四川省人民医院 |
| 邯郸市第一医院 |
| 潍坊呼吸病医院 |
| 云南省第一人民医院 |
| 山西省人民医院 |
| 内蒙古医学院第三附属医院 |
| 河北衡水哈励逊国际和平医院 |
| 海南省人民医院 |
| 青海省人民医院 |
| 贵州省人民医院 |
| 华北理工大学附属医院 |
| 福建省泉州市第一医院 |
| 锦州医科大学附属第一医院 |
| 首都医科大学附属复兴医院 |
| 淄博市立医院 |
| 山西省太原市中心医院 |
| 上海市肺科医院 |
| 新疆医科大学第三附属医院 |
| 山西医学科学院山西大医院 |
| 天津市海河医院 |
| 战略支援部队特色医学中心 |
| 河北医科大学第三医院 |
| 北京积水潭医院 |
| 无锡市人民医院 |
| 新疆维吾尔自治区中医医院 |
| 安徽省胸科医院 |
| 空军军医大学唐都医院 |
| 广东省人民医院 |
| 复旦大学附属华山医院 |
| 首都医科大学附属北京安贞医院 |
| 中国人民解放军总医院第一医学中心 |
| 宁夏医科大学总医院 |
| 河南省焦作市第二人民医院 |
| 首都医科大学附属北京同仁医院 |
| 南方医科大学南方医院 |
| 南昌大学第二附属医院 |
| 北京市大兴区人民医院 |
| 上海交通大学医学院附属新华医院 |
| 内蒙古自治区人民医院 |
| 南昌大学第一附属医院 |
| 中国医科大学附属盛京医院 |
| 西安交通大学第一附属医院 |
| 河北医科大学第一医院 |
| 广西壮族自治区人民医院 |
| 北京市顺义区医院 |
| 复旦大学附属中山医院 |
| 中山大学附属第三医院 |
| 粤北人民医院 |
| 首都医科大学附属北京世纪坛医院 |
| 中国科学院大学附属北京怀柔医院 |
| 首都医科大学附属北京儿童医院 |
| 天津市第一中心医院 |
| 华中科技大学同济医学院附属同济医院 |
| 兰州大学第二附属医院 |
| 西藏自治区第二人民医院 |
| 唐山工人医院 |
| 中日友好医院 |
